Ген-супрессор опухолей
Ген-супрессор опухолей (антионкоген, опухолевый супрессор) — ген, продукт которого обеспечивает профилактику опухолевой трансформации клеток[1]. Белковые продукты генов-супрессоров называют белками-супрессорами или антионкобелками. Кроме того, антионкогены могут кодировать и микроРНК[2]. Гены-супрессоры обычно обнаруживаются при инактивирующих мутациях, которые фенотипически проявляются в формировании опухолей. Функционально гены-супрессоры противоположны онкогенам и часто негативно регулируют деление и рост клеток, а также уход от апоптоза. Наиболее известными белками-супрессорами являются p53, pRb и PTEN.
История открытия и развития представлений о генах-супрессорах опухолей
[править | править код]Хотя наследственная предрасположенность к развитию злокачественных опухолей была известна давно, только после повторного открытия законов Менделя в 1900 году стало возможным научное объяснение этого факта. К этому времени уже было известно, что клетки опухолей имеют изменённый набор хромосом. Теодор Бовери внёс вклад в понимание генетики рака: он предположил, что есть хромосомы, которые стимулируют деление клеток, и есть хромосомы, которые его ингибируют[3]. Сегодня мы знаем, что гены обоих типов действительно существуют.
Известные гены-супрессоры опухолей
[править | править код]RB1
[править | править код]
TP53
[править | править код]
BRCA1
[править | править код]CDKN1A
[править | править код]Ген CDKN1A человека кодирует ингибитор циклинзависимой киназы. Этот белок также известен под названиями p21, Cip1, Waf1. Он связывается с комплексами циклин/циклинзависимая киназа (в первую очередь CDK1 и CDK2) и модулирует их активность. Конкретный эффект зависит от концентрации ингибитора: в низких концентрациях p21 стимулирует пролиферацию, в более высоких — приводит к остановке клеточного цикла в G1-фазе. Кроме того, p21 обеспечивает защиту клетки от апоптоза. То есть в зависимости от условий CDKN1A может выступать в роли антионкогена или онкогена[4].
Ген CDKN1A как правило не инактивируется полностью в злокачественных опухолях. Точная роль p21 в канцерогенезе до конца пока не установлена. Исследования показывают, что при некоторых типах опухолей потеря p21 является признаком плохих шансов на выживание. Однако известны ситуации, когда повышенная концентрация этого белка в клетках положительно коррелирует с агрессивностью опухоли и её способностью к метастазированию. Это особенно относится к тем случаям, когда p21 накапливается в цитоплазме, а не в ядре клетки[4].
CDKN1B
[править | править код]Ген CDKN1B человека кодирует ещё один ингибитор циклинзависимой киназы — CDKN1B, или p27 (Kip1). Этот белок регулирует течение клеточного цикла, отвечает за его остановку в G1-фазе. CDKN1B подавляет активность комплексов циклин А/циклинзависимая киназа 2 и циклин Е/циклинзависимая киназа 2.
Мутации в гене CDKN1B обуславливают предрасположенность к развитию множественных опухолей эндокринных желёз у человека и крыс[5]. Это заболевание, описанное на примере одной семьи, получило название множественной эндокринной неоплазии IV типа.
Была установлена связь между определёнными аллельными вариантами гена CDKN1B и предрасположенностью к раку предстательной железы. Один из вариантов однонуклеотидного полиморфизма являются замены 326T/G (V109G). Показано, что гомозиготность по варианту 326T ассоциированна с повышенным риском развития распространённой карциномы простаты. Другим примером является полиморфизм −79C/T, при этом наличие в генотипе человека аллели C сопряжено с повышенным риском развития рака простаты и других органов[6].
PTEN
[править | править код]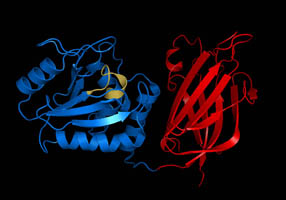
Ген PTEN у человека кодирует одноимённую фосфатазу PTEN (англ. phosphatase and tensin homologue), которая активна в отношении как белковых, так и липидных субстратов. Впервые этот ген был идентифицирован, как часто мутированный в различных видах раковых опухолей[7][8].
PDCD5
[править | править код]Примечания
[править | править код]- ↑ Benjamin Lewin. Chapter 30: Oncogenes and cancer // Genes VIII. — Upper Saddle River, NJ: Pearson Prentice Hall, 2004. — ISBN 0131439812.
- ↑ Lee Y. S., Dutta A. MicroRNAs in cancer. (неопр.) // Annu Rev Pathol.. — 2009. — Т. 4. — С. 199—227. — PMID 18817506. Архивировано 17 февраля 2022 года.
- ↑ Berger A. H., Knudson A. G., Pandolfi PP. A continuum model for tumour suppression. (англ.) // Nature : journal. — 2011. — Vol. 476. — P. 163—169. — doi:10.1038/nature10275. — PMID 21833082.
- ↑ 1 2 Warfel N. A., El-Deiry W. S. p21WAF1 and tumourigenesis: 20 years after // Curr Opin Oncol. Jan;25(1). — 2013. — Т. 25, вып. 1. — С. 52—58. — doi:10.1097/CCO.0b013e32835b639e. — PMID 23159848.
- ↑ Pellegata N. S., Quintanilla-Martinez L., Siggelkow H., Samson E., Bink K., Höfler H., Fend F., Graw J., Atkinson M. J. Germ-line mutations in p27Kip1 cause a multiple endocrine neoplasia syndrome in rats and humans // Proc Natl Acad Sci U S A. — 2006. — Т. 103, вып. 42. — С. 15558—15563. — PMID 17030811. Архивировано 25 мая 2021 года.
- ↑ Chang B. L., Zheng S. L., Isaacs S. D., Wiley K. E., Turner A., Li G., Walsh P. C., Meyers D. A., Isaacs W. B., Xu J. A polymorphism in the CDKN1B gene is associated with increased risk of hereditary prostate cancer // Cancer Res. — 2004. — Т. 64, вып. 6. — С. 1997—1999. — PMID 15026335. Архивировано 11 июля 2015 года.
- ↑ Li J., Yen C., Liaw D., Podsypanina K., Bose S., Wang S. I., Puc J., Miliaresis C., Rodgers L., McCombie R., Bigner S. H., Giovanella B. C., Ittmann M., Tycko B., Hibshoosh H., Wigler M. H., Parsons R. PTEN, a putative protein tyrosine phosphatase gene mutated in human brain, breast, and prostate cancer (англ.) // Science : journal. — 1997. — Vol. 275, no. 5308. — P. 1943—1947. — doi:10.1126/science.275.5308.1943. — PMID 9072974.
- ↑ Steck P. A., Pershouse M. A., Jasser S. A., Yung W. K., Lin H., Ligon A. H., Langford L. A., Baumgard M. L. , Hattier T., Davis T., Frye C., Hu R., Swedlund B., Teng D. H., Tavtigian S. V. Identification of a candidate tumour suppressor gene, MMAC1, at chromosome 10q23.3 that is mutated in multiple advanced cancers (англ.) // Nat Genet. : journal. — 1997. — Vol. 15, no. 4. — P. 356—362. — doi:10.1038/ng0497-356. — PMID 9090379.